Клеточные мембраны
Клеточные мембраны
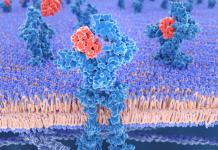
Изображение клеточной мембраны. Маленькие голубые и белые шарики соответствуют гидрофильным «головкам» липидов, а присоединённые к ним линии - гидрофобным «хвостам». На рисунке показаны только интегральные мембранные белки (красные глобулы и желтые спирали). Желтые овальные точки внутри мембраны - молекулы холестерола Желто-зеленые цепочки бусинок на наружной стороне мембраны - цепочки олигосахаридов , формирующие гликокаликс
Биологическая мембрана включает и различные белки : интегральные (пронизывающие мембрану насквозь), полуинтегральные (погруженные одним концом во внешний или внутренний липидный слой), поверхностные (расположенные на внешней или прилегающие к внутренней сторонам мембраны). Некоторые белки являются точками контакта клеточной мембраны с цитоскелетом внутри клетки, и клеточной стенкой (если она есть) снаружи. Некоторые из интегральных белков выполняют функцию ионных каналов, различных транспортеров и рецепторов .
Функции биомембран
- барьерная - обеспечивает регулируемый, избирательный, пассивный и активный обмен веществ с окружающей средой. Например, мембрана пероксисом защищает цитоплазму от опасных для клетки пероксидов . Избирательная проницаемость означает, что проницаемость мембраны для различных атомов или молекул зависит от их размеров, электрического заряда и химических свойств. Избирательная проницаемость обеспечивает отделение клетки и клеточных компартментов от окружающей среды и снабжение их необходимыми веществами.
- транспортная - через мембрану происходит транспорт веществ в клетку и из клетки. Транспорт через мембраны обеспечивает: доставку питательных веществ, удаление конечных продуктов обмена, секрецию различных веществ, создание ионных градиентов, поддержание в клетке соответствующего pH и ионной концентрации, которые нужны для работы клеточных ферментов.
Частицы, по какой-либо причине не способные пересечь фосфолипидный бислой (например, из-за гидрофильных свойств, так как мембрана внутри гидрофобна и не пропускает гидрофильные вещества, или из-за крупных размеров), но необходимые для клетки, могут проникнуть сквозь мембрану через специальные белки-переносчики (транспортеры) и белки-каналы или путем эндоцитоза .
При пассивном транспорте вещества пересекают липидный бислой без затрат энергии, путем диффузии. Вариантом этого механизма является облегчённая диффузия , при которой веществу помогает пройти через мембрану какая-либо специфическая молекула. У этой молекулы может быть канал, пропускающий вещества только одного типа.
Активный транспорт требует затрат энергии, так как происходит против градиента концентрации. На мембране существуют специальные белки-насосы, в том числе АТФаза , которая активно вкачивают в клетку ионы калия (K+) и выкачивают из неё ионы натрия (Na+).
- матричная - обеспечивает определенное взаиморасположение и ориентацию мембранных белков, их оптимальное взаимодействие;
- механическая - обеспечивает автономность клетки, ее внутриклеточных структур, также соединение с другими клетками (в тканях). Большую роль в обеспечение механической функции имеют клеточные стенки, а у животных - межклеточное вещество.
- энергетическая - при фотосинтезе в хлоропластах и клеточном дыхании в митохондриях в их мембранах действуют системы переноса энергии, в которых также участвуют белки;
- рецепторная - некоторые белки, находящиеся в мембране, являются рецепторами (молекулами, при помощи которых клетка воспринимает те или иные сигналы).
Например, гормоны, циркулирующие в крови, действуют только на такие клетки-мишени, у которых есть соответствующие этим гормонам рецепторы. Нейромедиаторы (химические вещества, обеспечивающие проведение нервных импульсов) тоже связываются с особыми рецепторными белками клеток-мишеней.
- ферментативная - мембранные белки нередко являются ферментами. Например, плазматические мембраны эпителиальных клеток кишечника содержат пищеварительные ферменты.
- осуществление генерации и проведения биопотенциалов.
С помощью мембраны в клетке поддерживается постоянная концентрация ионов: концентрация иона К+ внутри клетки значительно выше, чем снаружи, а концентрация Na+ значительно ниже, что очень важно, так как это обеспечивает поддержание разности потенциалов на мембране и генерацию нервного импульса .
- маркировка клетки - на мембране есть антигены, действующие как маркеры - «ярлыки», позволяющие опознать клетку. Это гликопротеины (то есть белки с присоединенными к ним разветвленными олигосахаридными боковыми цепями), играющие роль «антенн». Из-за бесчисленного множества конфигурации боковых цепей возможно сделать для каждого типа клеток свой особый маркер. С помощью маркеров клетки могут распознавать другие клетки и действовать согласованно с ними, например, при формировании органов и тканей. Это же позволяет иммунной системе распознавать чужеродные антигены.
Структура и состав биомембран
Мембраны состоят из липидов трёх классов: фосфолипиды , гликолипиды и холестерол . Фосфолипиды и гликолипиды (липиды с присоединёнными к ним углеводами) состоят из двух длинных гидрофобных углеводородных «хвостов», которые связаны с заряженной гидрофильной «головой». Холестерол придаёт мембране жёсткость, занимая свободное пространство между гидрофобными хвостами липидов и не позволяя им изгибаться. Поэтому мембраны с малым содержанием холестерола более гибкие, а с большим - более жёсткие и хрупкие. Также холестерол служит «стопором», препятствующим перемещению полярных молекул из клетки и в клетку. Важную часть мембраны составляют белки, пронизывающие её и отвечающие за разнообразные свойства мембран. Их состав и ориентация в разных мембранах различаются.
Клеточные мембраны часто асимметричны, то есть слои отличаются по составу липидов, переход отдельной молекулы из одного слоя в другой (так называемый флип-флоп ) затруднён.
Мембранные органеллы
Это замкнутые одиночные или связанные друг с другом участки цитоплазмы , отделённые от гиалоплазмы мембранами . К одномембранным органеллам относятся эндоплазматическая сеть , аппарат Гольджи , лизосомы , вакуоли , пероксисомы ; к двумембранным - ядро , митохондрии , пластиды . Снаружи клетка ограничена так называемой плазматической мембраной. Строение мембран различных органелл отличается по составу липидов и мембранных белков.
Избирательная проницаемость
Клеточные мембраны обладают избирательной проницаемостью: через них медленно диффундируют глюкоза , аминокислоты , жирные кислоты , глицерол и ионы , причем сами мембраны в известной мере активно регулируют этот процесс - одни вещества пропускают, а другие нет. Существует четыре основных механизма для поступления веществ в клетку или вывода их из клеки наружу: диффузия , осмос , активный транспорт и экзо- или эндоцитоз . Два первых процесса носят пассивный характер, то есть не требуют затрат энергии; два последних - активные процессы, связанные с потреблением энергии.
Избирательная проницаемость мембраны при пассивном транспорте обусловлена специальными каналами - интегральными белками. Они пронизывают мембрану насквозь, образовывая своего рода проход . Для элементов K, Na и Cl есть свои каналы. Относительно градиента концентрации молекулы этих элементов движутся в клетку и из неё. При раздражении каналы натриевых ионов раскрываются, и происходит резкое поступление в клетку ионов натрия. При этом происходит дисбаланс мембранного потенциала. После чего мембранный потенциал восстанавливается. Каналы калия всегда открыты, через них в клетку медленно попадают ионы калия .
Ссылки
- Bruce Alberts, et al. Molecular Biology Of The Cell . - 5th ed. - New York: Garland Science, 2007. - ISBN 0-8153-3218-1 - учебник по молекулярной биологии на англ. языке
- Рубин А.Б. Биофизика, учебник в 2 тт. . - 3-е издание, исправленное и дополненное. - Москва: издательство Московского университета, 2004. - ISBN 5-211-06109-8
- Геннис Р. Биомембраны. Молекулярная структура и функции: перевод с англ. = Biomembranes. Molecular structure and function (by Robert B. Gennis). - 1-е издание. - Москва: Мир, 1997. - ISBN 5-03-002419-0
- Иванов В.Г., Берестовский Т.Н. Липидный бислой биологических мембран. - Москва: Наука, 1982.
- Антонов В.Ф., Смирнова Е.Н., Шевченко Е.В. Липидные мембраны при фазовых переходах. - Москва: Наука, 1994.
См. также
- Владимиров Ю. А., Повреждение компонентов биологических мембран при патологических процессах
Wikimedia Foundation . 2010 .
Смотреть что такое "Клеточные мембраны" в других словарях:
У этого термина существуют и другие значения, см. Мембрана Изображение клеточной мембраны. Маленькие голубые и белые шарики соответствуют гидрофильным «головкам» липидов, а присоединённые к ним линии гидрофобным «хвостам». На рисунке показаны… … Википедия
- (от лат. membrana кожица, перепонка), сложные высокоорганизованные надмоле кулярные структуры, ограничивающие клетки (клеточные, или плазматич., мембраны) и внутриклеточные органоиды митохондрии, хлоропласты, лизосомы и др. Представляют собой… … Химическая энциклопедия
У этого термина существуют и другие значения, см. Мембрана Изображение клеточной мембраны. Маленькие голубые и белые шарики соответствуют гидрофильным «головкам» липидов, а присоединённые к ним линии гидрофобным «хвостам». На рисунке показаны… … Википедия
Живые клетки, как и организм в целом - открытая система с постоянным обменом вещества и энергии. В процессе этого обмена происходит проникновение веществ в клетке и из клетки.
С образованием в клетках электрических потенциалов, нарушение клеточной проницаемость приводит к патологическим изменениям, лечебное действие врача с назначением препарата связано с проникновением этих веществ в клетку и воздействие на ее функциональные свойства.
Задачи
- Изучение механизма проникновения веществ через мембрану
- Определение распределения веществ между внутриклеточной и внеклеточной средой.
Методы изучения проницаемости
- Объемный метод. Основан на явлении осмоса. Определение массы клеток до и после помещения их в гипертонический раствор изучаемого вещества. Вещество проникает в клетку и увеличивается объем(из-за воды). Метод центрифугирования - определение эритроцитарной массы с помощью него. При фотометрии изменяется показатель проникновения веществ в клетку.
- Индикаторный метод. Он сводится к определению прижизненной окраски. Качественный метод, т.к. поступление вещества определяется по изменению окраски индикатора, который предварительно вводится в клетку. Используется для кислот и щелочей. Метод колориметрии может дать не только качественную, но и количественную оценку. Недостаток - малые концентрации плохо улавливаются, а большие - губительны для клетки.
- Химический метод - исследует качественное и количественное определение веществ в клетках и окружающей среде.
- Изотопный метод изучения проницаемости. Он позволяет изучить потоки любых веществ поступающих как в клетку, так и из нее. Метод позволяет работать на живых объектах и использовать малые концентрации изучаемых веществ. Позволяет изучать проникновение не только чужеродных веществ, но и веществ - компонентов данной клетки.
- Метод измерения электропроводности. Применяется для измерения ионов. По изменению низкочастотного тока позволяет судить о проницаемости.
Физические факторы, обусловливающие пассивное проникновение веществ через мембрану.
- Концентрационный(химический) градиент
- Электрохимический градиент
- Электростатический градиент(для процессов фильтрации)
- Осмотический градиент
- Градиент растворимости на границе двух несмешивающихся фаз, например липидной и водной
Они обеспечивают пассивное движение веществ.
Активная проницаемость, идет с затратами энергии, перенос осуществляется против градиента концентрации.
Основным видом пассивного транспорта будет являться диффузия - простая(через поры в липидном бислое, через белковую пору, либо через поры в липидном бислое) и облегченная с (фиксированным или подвижным переносчиком). К пассивному транспорту относится осмос и фильтрация - перемещения вещества и растворителя.
Диффузия является основным путем переноса веществ. Диффузия - самопроизвольный процесс проникновения веществ из области большей в область с меньшей концентрацией в результате теплового хаотического движения атомов и молекул. Кинетическая энергия - mV2 / 2.
Если частица имеет заряд включается еще электрохимический градиент.
Уравнение Нернста-Планка
Jm = URT dC/dx - UCZF dф/dx
U - подвижность частиц
С - концентрация
R - газовая постоянная
T- температура
Z - заряд иона
F - число Фарадея
Dx - толщина мембраны
dC/dx - градиент концентрации
dф/dx - градиент электрохимического потенциала
Закон Фика
Jm = -D dC/dx Jm = P(C1-C2)
Если нет заряда.
P - коэффициент проницаемости мембраны
K - коэффициент распределения
Вещества в процессе диффузии проходят через поры мембраны - водорастворимые, полярные соединения и электролиты. Органические вещества проходят за счет растворения в липидах. Зависимость растворения веществ в липидах исследовалось Овертоном. Он показал если есть карбоксильные, гидроксильные и аминогруппы, то это ухудшает проникновение через мембрану. Присутствие же метиловых, этиловых и фенильных групп наоборот облегчает проникновение веществ в клетку. Они не полярные и это увеличивает растворения этих веществ в липидах.
Коэффициент распределения показывает отношение растворимости веществ в жирах к растворимости этих веществ в воде. Чем выше этот коэффициент, тем легче проникают вещества в клетку, вне зависимости от размеров молекулы. Если вещества имеют одинаковый коэффициент распределения, то более мелкие молекулы будут проникать легче чем крупные.
Водорасстворимые вещества проходят через поры мембран. Для того чтобы пройти через пору, вещество должно преодолеть определенные силы, которые препятствуют этому. Вещество должно освободится от водной или сольватной оболочки, раздвинуть поверхностный молекулярный слой на границе клетки и омывающего раствора, преодолеть взаимодействие своих полярных групп и полярных групп поры мембран, преодолеть энергетический барьер, создаваемый на поверхности цитоплазмы ионами и коллоидами.
Проницаемость ионов через мембрану .
Она зависит от следующих факторов.
- Размер кристаллического радиуса
- Размер гидратной оболочки и ее прочности
- От валентности иона, которая определяется величиной заряда
- От фазовых переходов мембраны из жидкокристаллического состояния в гель и обратно. Радиус гидратирвоанного иона будет определяться кристаллическим радиусом и наличием одной или нескольких гидратных оболочек. Водная оболочка у анионов на 18% компактнее чем у катионов. Анионы лучше проходят через мембрану. При прохождении через пору ион сохраняет одну гидратную оболочку, а остальные замещаются стенками поры. Легче это происходит, если меньше энергия гидратации.
На проникновение в клетку будет влиять заряд, т.к. происходит взаимодейтсвие с порой. Одновалентные ионы лучше чем 2х и чем 3х. Натрий, калий лучше, кальций, магний - лучше, совсем плохо - железо.
Состояние мембраны. Поры жидкого кристалла и геля. Кристалл(занимает большую плотность, за счет раздвижения жирных хвостов - 0,58 и 3,9). Гель - жирные хвосты параллельно расположены и площадь уменьшается до 0,48, но увеличивается толщина увеличивается до 4,7. Транс конфигурация - вытянуты и отклонения хвостов в Гош-транс-гош конфигурации.
В жидкокрситалическом состоянии в мембране есть микрополости - kink петля. эти микрополости захватываются ионы, вода и они могут перемещаться вдоль мембраны и мембрана осуществляет перенос.
Процесс диффузии может облегчаться за счет наличия переносчиков. Особенность облегченной диффузии, также как по градиенту концентрации, только быстрее. Обладает свойством транспортного максимума - нарастания скорости проницаемости вещества зависит от свободных переносчиков, но когда все переносчики заняты, скорость уменьшается. Увеличение скорости облегченной диффузии идет до определенного момента. Возможна конкуренция переносимых веществ, когда к переносчику присоединяются разные вещества.
Процесс фильтрации - видение раствора через пору в мембране под действием градиента давления.
Подчиняется уравеннию Пуазейля
dV/dt = пи R4(p1-p2) / 8lή
dV/dt=(p1-p2)/ w W=8lή/пи R4
r4 - радиус поры
l- длина поры
ή - вязкость жидкости
V - объем фильтрованной жидкости
W - гидлравлическое сопротивление
В капиллярах клубочков почек - булки не могут пройти через фильтр, они остаются в плазме и создают осмотическое давлении. Фильтрованная жидкость - создает гидростатическое давление, препядствующее фильтрации.
Большое значение в организме имеет осмос. Вода по законам осмоса из раствора с меньшей концентрацией веществ в раствор с большей концентрацией. Осмос - это диффузия молекул воды. Идее по градиенту осмотического давления (пи)
Пи=iRCT i-изотонический коэффициент диссоциации молекул.
Осмоляльность. Осмоль.
При определении концентрации раствора в показателях чатсиц вместо гарммов - осмоль.
Один осмоль является 1 грамм-молекулой растворенного вещества.
Раствор, который содержит 1 / 1000 осмоля на 1 кг воды, имеет осмоляльность 1 милиосмоль(мосм) на 1 кг. Нормальная осмоляльность внеклеточной и внутриклеточной жидкости равна примерно 300 мосм на 1 кг
Осмолярность
В связи со сложностью измерения воды в растворе в килограммах, что необходимо для определения осмоляльности, вместо этого использую осмолярность - концентрацию выражаемую числом осмолей на 1 л раствора, а не на 1 кг.
Различия в покащателях осмоляльности и осмолярности составляют менее 1%
Проницаемость мембран для воды
- Осмотический градиент
- Гидрсотатический градиент
- Электрический градиент
- Онкотическое давление белков. Обеспечивает аномальный осмос.
Неодинаковая скорость проникновения катионов и анионов создает диффузионную разность потенциалов. Эта разность потенциалов может влиять на проникновение воды. Аномальный осмос может быть положительным и отрицательным. При положительном осмосе - вода движется по осмотическому градиенту, но с дополнительным ускорением, а при отрицательном аномальном осмосе вода переносится против осмотического градиента, но по градиенту электрической разности потенциала.
Теории транспорта воды
Теория Вант-Гофа - проникновение воды через поры тепловым движением ее молекул.
Проникновение воды в виде пары.
Мембраны хорошо проницаемы для газов независимо от их природы. Газы не имеют заряд. Газы могут растворяться в липидах.
Проницаемость для кислот и щелочей зависит от степени их диссоциации. Проницаемость алкалоидов тоже. Не диссоциируемые - хорошо проходят через мембрану, т.к. растворяются в липидах, а диссоциируемые не могут пройти через поры мембран из за большой величины.
Активный транспорт - связан с затратой энергии, и против градиента.
Первично активный и вторично активный транспорт.
Первично активный транспорт - насосные механизмы для переноса ионов мембран.
Фермент может находитcя в 2х конформационных состояниях - E1/E2. Может присоединится к альфа суб единице в состоянии Е1 три единицы. Происходит распад АТФ до АДФ и неорганического фосфата. Фосфатная группа переносится на аспарагин в 376 положении. Белок при фосфолилировании осуществляет поворот и три иона изнутри оказываются снаружи. Альфа суб единица после поворота приобретает сродство к калию. И захватывает 2 иона калия. Алее дефосфолилирование и новое конформационное изменение переход в Е2 и 2 калия возвращается внутрь.
Этот транспорт поддерживает нормальное распределение натрия и калия во внутриклеточной и вне жидкости. Также +заряд на наружной поверхности мембраны. С выносом 3х ионов натрия из клетки удаляется вода, т.е. поддерживается водный баланс клетки.
Вторчино активный транспорт используется для переноса органических соединений, необходимых для клетки и этот вторично активный транспорт осуществляется с помощью переносчиков = 2 натрий + глюкоза(например). Движется в клетке по градиенту натрия в клетку. Здесь энергия не расходуется, но глюкоза из клетки должна уйти в кровь - путем простой диффузии, а натрий из клетки удаляется натрий-калий АТФазой. Это нужно для поддержания концентрационного градиента.
Активные процессы транспорта вещества связаны также с эндоцитозом - фагоцито - перенос плотных частиц и пиноцитоз - если переносятся жидкости. Этот процесс может быть специфическим и не. Специфический - если мембрана сама отбирает с помощью специальных рецепторных белком мембраны. Мембрана образует складку, которая смыкается и переходит в пузырек, он создает первичную эндосому, в которую включены вещество, белок. Из первичной эндосомы удаляется белок(клатрин) и первичная эндосома переходит во вторичную эндосому, и она сливается с лизосомой.
Гормоны, которые не могут проходить через мембрану, взаимодействуют с рецепторами. А др. часть гормонов, растворимых в жирах, проникает внутрь клетки и взаимодействуют с цитозольными рецепторами.
Бимолекулярный слой фосфолипидов составляет основу любой клеточной мембраны. Непрерывность его определяет барьерные и механические свойства клетки. В процессе жизнедеятельности непрерывность бислоя может нарушаться с образованием структурных дефектов типа сквозных гидрофильных пор. Вполне естественно ожидать при этом. Изменяются при этом все функции клеточной мембраны, включая проницаемость и стабильность.
Фосфолипиды, составляющие основу клеточных мембран, относятся к жидким кристаллам. Как в любом реальном кристалле, в пленке из фосфолипидов могут быть дефекты, в месте которых и развиваются основные события структурных перестроек. Виды дефектов многообразны, но и наиболее естественным для бислоя является дефект типа сквозной гидрофильной поры.
В липидной бимолекулярной пленке клеточной мембраны поры появляются, если исключить чисто механические повреждения, в результате тепловых флуктуации поверхности бислоя, электрического пробоя, замораживания пленки, действия поверхностно-активных веществ, осмотического давления, перекисного окисления липидов и др. Один из наиболее типичных и хорошо изученных примеров дестабилизации биологических мембран - гемолиз эритроцитов. Это явление включает на начальном этапе набухание клеток в гипотонической среде в результате действия сил осмотического давления. Во время набухания клетки мембрана растягивается, что обусловливает рост мембранного натяжения. При определенном пороговом уровне натяжения появляются гидрофильные липидные поры. Размеры пор достаточны для выхода молекул гемоглобина и низкомолекулярных веществ. Выход веществ сопровождается в свою очередь снижением разности осмотического давления, при этом натяжение мембраны уменьшается и поры залечиваются. Белки цитоскелета позволяют эритроциту сохранить форму, при этом образуется так называемая тень эритроцита. Тень сохраняет осмотическую активность и таким образом процесс дестабилизации приобретает циклический характер. Полного механического разрушения клетки подобного мыльному пузырю в этом случае не происходит. В отсутствие цитоскелета или его недостаточного развития механическая прочность клетки целиком определяется судьбой липидных пор. Если пора имеет размер меньше критического, то она залечивается. В противном случае неограниченный рост поры приводит к разрушению мембраны.
Модель критической поры. Рассмотрим модель липидной поры (рис. 15). Будем считать, что боковая поверхность поры имеет форму кругового цилиндра. Более того, предположим, что боковая поверхность цилиндра изогнута и имеет радиус кривизны h/2. Радиус поры равен r. Как видно, липидный бислой в целом является плоским, а пора имеет два радиуса кривизны h/2 и r. Искривление поверхности на границе раздела липид-вода сопровождается появлением добавочного давления, называемого лапласовым и равного
P = 2s 1 /r
где s 1 - межфазное натяжение внутри поры, r- радиус кривизны.
Рис.15. Строение гидрофильной липидной поры: h -толщина липидного бислоя; h/2 - радиус кривизны стенки; r - радиус поры.
В рассматриваемой модели таких радиусов два (h/2 и r) и, следовательно, два давления. Одно из них Р (h/2) способствует расширению, а другое Р (r) - сжатию поры. Дальнейшая судьба поры зависит от соотношения этих двух давлений. Если Р (h/2) > Р (r), пора будет расширяться, а если Р (h/2) меньше Р (r), то пора будет затекать.
Рассмотрим энергетику поры. Как установлено выше, на границе поры действуют две противоположные силы, одна из которых - краевое линейное натяжение периметра поры - способствует росту поры, а вторая сила - поверхностное натяжение бислоя - вызывает сжатие поры. Краевая энергия поры пропорциональна первой степени радиуса и увеличивает суммарную энергию, энергия поверхностного натяжения пропорциональна квадрату радиуса и снижает суммарную энергию. В результате суммарная энергия Е (r) равна
E(r) = 2pr 2 s
где первый член определяется энергией кромки поры с линейным натяжением g, а второй - энергией поверхностного натяжения s.
С учетом неустойчивости равновесия можно утверждать, что появление пор с r>r* (r*=g/s) пора будет затекать и стабильность мембраны сохранится. Таков критерий стабильности липидной бислойной мембраны.
Электрический пробой мембраны. Биологические мембраны находятся под действием электрического поля большой напряженности, создаваемого диффузией ионов через мембрану и электрогенными ионными насосами. Разность потенциалов между цитоплазмой и внеклеточной средой достигает порядка 0,1 В, толщина мембраны не превышает 10 нм, значит напряженность поля равна 10 7 В/м. Мембрана является более совершенным электрическим изолятором, чем многие жидкие изоляторы, применяемые в технике. Мембранный потенциал в живой клетке может достигать 0,2 В (пресноводные водоросли, бактерии, энергизированные митохондрии). В возбудимых нервных и мышечных клетках происходит кратковременная реполяризация мембраны с ростом амплитуды потенциала. Однако пробой клеточной мембраны собственным мембранным потенциалом маловероятен. В то же время рост мембранного потенциала в результате воздействия внешним электрическим полем может достигать величины, превышающей пороговую для электрического пробоя. При этом появляются структурные дефекты типа сквозных липидных пор. Разработанная методика электрического пробоя клеточных мембран получила название электропорации и широко применяется в биотехнологии.
В физике под электрическим пробоем понимают резкое увеличение силы электрического тока в первоначально слабопроводящей среде. В живой клетке такой средой служит бимолекулярный слой липида. Для липидного бислоя в жидкокристаллическом состоянии величина мембранного потенциала не может быть меньше 0,23 В. Стабильность бислойных мембран определяется вероятностью появления пор критического радиуса. Очевидно, что любой фактор, снижающий высоту энергетического барьера, будет увеличивать эту вероятность. К таким факторам следует отнести сниение краевой энергии поры у, рост поверхностного натяжения и рост мембранного потенциала. Электрический пробой сопровождается появлением широкого спектра липидных пор различного радиуса, включая радиусы ионоселективных белковых каналов. В настоящее время метод воздействия внешним электрическим полем является одним из основных в современной биотехнологии. Известно его применение с целью увеличения пористости мембран (электропорация), введения ДНК (электротрансфекция), освобождение клеток от крупных молекул (электропермеабилизация), слияния клеток (электрослияние).
Температурный фазовый переход мембранных липидов. Замораживание липидного бислоя в результате фазового перехода из жидкокристаллического состояния в гель сопровождается появлением липидных пор. Очевидно, что, как и в случае с электрическим пробоем, судьбу мембраны будет определять соотношение радиусов образовавшихся пор и критических пор для данного состояния бислоя.
Критический радиус поры в гель-состоянии значительно меньше по сравнению с жидкокристаллическим состоянием и по абсолютной величине не превышает 2 нм. Сохранение длительной устойчивости липидного бислоя в гель-состоянии свидетельствует о том, что существующие поры и поры, возникающие при фазовом переходе, имеют размеры меньше 2 нм. Замораживание мембранных липидов в ходе фазового перехода, эквивалентно электрическому пробою мембраны внешним электрическим полем напряжением 0,5 В. Любое воздействие механической, физической или химической природы, затрагивающее поверхностное натяжение липидного бислоя, является фактором риска в стабилизации порсодержащих мембран. Развитие такого подхода позволяет получить количественный ответ на важный для биологии о вероятности разрушения или залечивания мембран при типичных стрессовых состояниях живой клетки.
Критический радиус пор в мембранах, находящихся в жидкокристаллическом состоянии при отсутствии внешних воздействий, достигает 9 нм. Эта величина настолько значительна, что вероятность механического разрыва клеточных мембран в физиологических условиях очень мала. Разрыв мембраны, находящейся в таком состоянии, возможен лишь тогда, когда пора приобретает размеры, соизмеримые с толщиной мембраны. Опыт показывает, что полное разрушение липидного бислоя возможно лишь при грубых механических манипуляциях или необратимом электрическом пробое липидов (жкс), гель-состоянии (гель), при электрическом пробое (эп), при сочетании гель-состояния с электрическим пробоем (гель+эп).
Размеры критических пор для липидного бислоя в жидкокристаллическом состоянии (9нм) значительно превышают размеры реальных пор. Мембраны в различных стрессовых состояниях обладают значительным запасом прочности, действие электрического пробоя и замораживания бислоя, аддитивно. Такой результат можно ожидать, следовательно, и при других сочетаниях физических и химических воздействий. Стрессовое воздействие таким образом, независимо от его физико-химической природы, может быть количественно оценено и его результат предсказан в рамках рассматриваемой модели. Модель формирования пор при фазовом переходе. Независимая оценка размера пор может быть получена путем исследования предложенной В.Ф. Антоновым и сотрудниками модели формирования пор. При фазовом переходе из жидкокристаллиеского состояния в гель по данным рентгеноструктурного анализа, происходит изменение толщины бислоя и площади на молекулу липида. Учитывая кооперативность фазового перехода, можно предположить, что молекулы в доменах, перешедших в гель-фазу, и остающихся в жидкокристаллическом состоянии, будут находиться в разных условиях. Относительно равновесного состояния молекулы в домене гель-фазы будут растянуты, а в жидкокристаллическом состоянии - сжаты. Появится упругое напряжение, которое приведет к нарушению структуры бислоя.
Липидные поры и проницаемость мембран. С точки зрения проницаемости липидные поры принципиально отличаются от белковых каналов своим происхождением и исключительной динамичностью. В то время как белковые каналы имеют строго определенные размеры, сохраняющиеся в течение всей жизни клетки, размеры лилидных пор в процессе затекания варьируют в широких пределах. Однако эта изменчивость; имеет предел. Если радиус поры меньше критического, то пора в процессе затекания должна пройти все промежуточные радиусы и достигнуть минимального размера. Вопрос о возможности полного затекания липидных пор остается открытым. Предполагается, что полному затягиванию поры препятствуют мощные силы гидратации, проявляющиеся при сближении стенок гидрофильных пор. Лшшдные поры в отличие от белковых ионных каналов не обладают выраженной избирательностью, что коррелирует с их сравнительно большими исходными размерами. Ясно, однако, что в процессе затекания липидные поры могут достигать сколь угодно малых размеров, в том числе сравнимых с размерами белковых ионных каналов, что может приводить к перераспределению ионных токов в мембране, например, при возбуждении. Известно далее, что после выключения стрессового воздействия бислойная липидная мембрана может вернуться в состояние с низкой проводимостью, что подразуевает достижение порами размера, недостаточного для прохождения гидратированных ионов. Таким образом, гидрофильные липидные поры универсальны в том отношении, что могут быть использованы клеткой для транспорта высокомолекулярных веществ, ионов и молекул воды.
Исследования проницаемости липидных пор развиваются в настоящее время в двух направлениях: в первом исследуются максимально большие поры, во втором, наоборот, - липидные поры минимального радиуса. В первом случае речь идет об электро-трансфекции - способе введения в живые клетки или липосомы молекул ДНК с целью переноса и внутриклеточного введения чужеродного генетического материала. Оказалось, что внешнее электрическое поле высокой напряженности способствует проникновению гигантской молекулы ДНК внутрь мембранной частицы. Максимальный размер критической поры соответствует жидкокристаллическому состоянию бислоя липидов в отсутствие внешнего электрического поля и равен 9 нм. Наложение внешнего электрического поля напряженностью 100 кВ/м понижает критический радиус поры до 1 нм за время 0,2 с. Поскольку при этом мембраны сохраняются, то размер липидных пор в них не превышает этого нижнего предела. Парадокс состоит в том, что эффективный диаметр статистического клубка ДНК, которая должна лопасть внутрь частицы, достигает 2000 нм. Поэтому молекула ДНК должна проникать через мембрану в виде расплетенной одиночной нити. Известно, что конец нити имеет диаметр 2 нм и таким образом только-только может войти в пору. Однако свободная диффузия нити ДНК в поре при этом вряд ли возможна. К сожалению, механизм этого явления до конца не ясен. Предполагается, в частности, что молекула ДНК способна расширить пору и таким образом проскользнуть через мембрану. Проникновению ДНК могут способствовать дополнительные силы электрофореза и электроосмоса с учетом суммарного отрицательного заряда молекулы ДНК. Не исключено, что поры с фиксированными в них концами молекулы ДНК играют роль якоря, удерживающего молекулу в определенном месте у поверхности мембраны везикулы, а сам процесс переноса является разновидностью пиноцитоза. Исследование этого интересного с точки зрения проницаемости явления продолжается,
Второе направление исследования проницаемости мембран с участием липидных пор связано с трансмембранным переносом молекул и ионов воды. Известное в биологии явление высокой водной проницаемости клеточных мембран полностью воспроизводится на искусственных липидных бислоях, что подразумевает участие в этом процессе гидрофильных липидных пор.
Основной вывод состоит в том, что стабильность липидного бислоя и клеточной мембраны, лишенной белкового каркаса, определяется липидными порами. Эти поры образуются в местах дефектов жидкокристаллической структуры липидного бислоя. Липидные поры возникают в результате тепловых флуктуации поверхности бислоя, а также могут рождаться при мембранном стрессе, сопровождающем фазовый переход мембранных липидов, при электрическом пробое и осмотическом лизисе. Судьба мембраны в этих случаях будет зависеть вероятностным образом от того, будет ли липидная пора превышать некоторый критический размер или нет. В первом случае мембрана порвется, во втором случае ее структура сохранится. При сохранении стабильности мембран поры залечиваются, пробегая при этом все промежуточные значения радиусов. Минимальные радиусы липидных пор могут стать сравнимыми с размерами избирательных белковых каналов, регулирующих в норме ионную проницаемость клеточных мембран. На последних этапах затекания липидные поры могут превращаться в водные поры, доступные только для молекул и ионов воды.
Мембранные методы очистки основаны на различной проницаемости мембран для компонентов очищаемой газовой смеси.[ ...]
Селективную проницаемость мембран в процессе ультрафильтрации объясняет чисто ситовой механизм разделения - частицы примесей, имеющие больший размер, чем размеры пор мембраны, через мембрану не проходят, через нее профильтровывается только вода.[ ...]
Селективность и проницаемость мембран должны рассматриваться во взаимосвязи с затратами на получение воздуха, обогащенного кислородом. Расходы на разделение воздуха зависят от проницаемости, селективности, геометрических параметров мембран, производительности модуля, стоимости электроэнергии и других факторов. Стоимость обогащенного кислородом воздуха оценивается по отношению к эквивалентно чистому кислороду, определяемому как количество чистого кислорода, необходимого для смешения с воздухом (21% кислорода) при получении того же количества и процентного содержания кислорода, которое получается в рассматриваемом газоразделительном процессе.[ ...]
Ультрафильтрация - мембранный процесс разделения растворов, осмотическое давление которых мало. Этот метод используется при отделении сравнительно высокомолекулярных веществ, взвешенных частиц, коллоидов. Ультрафильтрация по сравнению с обратным осмосом - более высокопроизводительный процесс, так как высокая проницаемость мембран достигается при давлении 0,2-1 МПа.[ ...]
Промывка твердых отходов 434, 425 Проницаемость мембран 273 Процеживание 197 сл.[ ...]
Ионы кальция оказывают большое влияние на мембранные структуры. На необходимость ионов Са2+ для стабилизации мембран указывалось достаточно давно. Было показано, что для образования поверхностной мембраны на эндоплазматической капле, изолированной из интерно-дальных клеток харовых водорослей, необходимо присутствие в окружающем растворе ионов Са2+. Присутствие Са2+ в концентрации 10 4 М способствовало образованию поверхностной мембраны на капле, хотя и недостаточно прочной; более прочная мембрана образовывалась при концентрации 10"3 М и особенно 10 2 М. При удалении ионов кальция (например, при обработке хелатами или при отсутствии Са2+ в среде) отмечается ослизнение корневых волосков, а также повышается проницаемость мембран к другим веществам. Ионы Са2+ изменяют и электрические свойства как искусственных, так и естественных мембран, умень-шая плотность заряда на мембранной поверхности. Недостаток Са приводит к возрастанию вакуолизации, изменению хромосом, разрыву мембран ЭПР и других внутриклеточных компартментов.[ ...]
С ростом концентрации разделяемого раствора проницаемость мембран уменьшается, с ростом давления - увеличивается. После процесса очистки получается фильтрат, обедненный на 90-99,5 °/о исходными соединениями, и концентрат, направляемый на дальнейшую переработку.[ ...]
Реакция на ацетилхолин и биогенные амины состоит в изменении проницаемости мембран к ионам и/или индукции синтеза вторичных посредников. Присутствие в растительной клетке и ее органеллах цАМФ, цГМФ, Са2+, а также ферментов синтеза и катаболизма подтверждает возможность локальной медиации.[ ...]
Так, под действием СВЧ ЭМИ (2,45 ГГц) обнаружено увеличение катионной проницаемости мембран эритроцитов при комнатной температуре, в то время как в отсутствие СВЧ ЭМИ подобный эффект наблюдается только при температуре 37 °С.[ ...]
Фонды метаболитов не равномерно распределены по клетке, а разделены мембранами и локализованы в отдельных отсеках (камерах, компартментах). Компартменты метаболических фондов клетки связаны между собой транспортными потоками. В соответствии с избирательной проницаемостью мембран происходит пространственное перераспределение интермедиатов и продуктов обмена. Например, в клетке запас АТФ поддерживается за счет "горизонтальных" связей процессов фотосинтетического и окислительного фосфоршшрования.[ ...]
Концентрация раствора. С ростом концентрации разделяемого раствора проницаемость мембран уменьшается вследствие увеличения осмотического давления растворителя и влияния концентрационной поляризации. При значении критерия Рейнольдса 2000-3000 концентрационная поляризация практически отсутствует, однако турбулизация раствора связана с его многократной рециркуляцией, т. е. с затратами энергии, и приводит к накоплению взвешенг ных частиц в растворе и появлению биологических обрастаний.[ ...]
Понижение температуры воды, ведущее к охлаждению рыб, ведет и к увеличению проницаемости мембран, которые теряют способность поддерживать ионные градиенты. При этом нарушается сопряженность ферментативных реакций, перестают работать ионные насосы, нарушается работа центральной и периферической нервной системы, угнетается работа кардиореспираторного аппарата, что в конечном счете может привести к развитию гипоксии. При перегреве или охлаждении рыб, возникающих в результате резкого изменения температуры в ограниченное время, определенная роль принадлежит осмотическим стрессам вследствие нарушения способности организма поддерживать определенную концентрацию ионов и белков в крови . Так, например, снижение температуры с 25 до 11°С вызывает у тиляпии, содержавшейся в пресной воде, развитие коматозного состояния, сопровождающегося снижением концентрации ионов натрия и хлора и общего белка крови . По мнению авторов, гибель рыб наступает из-за развития осморегуляторного коллапса и угнетения функции почёк. Косвенным подтверждением этого предположения может служить предотвращение температурной комы у рыб, содержащихся в разбавленной морской воде, что согласуется с более ранними наблюдениями повышения терморезистентности рыб вследствие добавления в воду ионов натрия, кальция и магния . Следует, однако, иметь в виду, что причины гибели рыб при повышенных или пониженных температурах различны и зависят от продолжительности и интенсивности температурного воздействия.[ ...]
Величина pH. Изменение первоначального значения pH обычно приводит к понижению проницаемости мембран . Влияние pH на селективность мембран невелико. Летучие кислоты плохо задерживаются мембранами, поэтому предварительная нейтрализация летучих кислот повышает селективность процесса разделения.[ ...]
При высоких концентрациях солей в трехкамерном электродиализаторе с инертными мембранами максимальный выход по току не превышает 20%.[ ...]
Получены положительные результаты очистки сточных вод от ОП-7 обратным осмосом при давлении 5 МПа. Проницаемость мембран составляла 5-20,8 л/(м2-ч) при концентрации ОП-7 в фильтрате 1-18 мг/л .[ ...]
ПАВ (алкилсульфаты) стимулируют размножение бактерий в наибольшей степени. Кроме того, ПАВ, изменяя проницаемость мембран живых клеток (С. С. Строев, 1965 и др.), возможно, способствуют лучшей усвояемости микробами пищевых веществ, содержащихся в воде.[ ...]
Природа растворенного вещества оказывает определенное влияние на селективность и в меньшей степени на проницаемость мембран. Это влияние заключается в том, что неорганические вещества задерживаются мембранами лучше, чем органические с той же молекулярной массой; среди родственных соединений, например, гомологов, лучше задерживаются вещества с большей молекулярной массой; вещества, образующие связи с мембраной, например, водородную, задерживаются мембраной тем лучше, чем менее прочна эта связь; селективность задержания высокомолекулярных соединений ультрафильтрацией тем больше, чем больше молекулярная масса растворенного вещества.[ ...]
Мембраны из ацетата целлюлозы могут работать в интервале pH 4,5-7, а из химически стойких полимеров - при pH 1 -14. Проницаемость мембран выбирается такой, чтобы обеспечивать проход воды, растворимых солей и задерживать масла. Размер пор в мембранах обычно составляет в пределах 2,5-10 нм. Установка оборудована вспомогательными трубопроводами для промывки мембран фильтратом или деминерализованной водой, снабжена контрольно-измерительными приборами и автоматическими устройствами.[ ...]
При значительном снижении внутриклеточной разности потенциалов до определенного порогового уровня наблюдается резкое изменение проницаемости мембран и обращение (реверсия) ионных потоков. Ионы кальция из наружной среды, окружающей клетку, поступают в нее, а ионы хлора и ионы калия выходят из клетки в омывающий раствор.[ ...]
Толерантность связана с внутренними факторами и включает такие метаболические процессы, как селективное поглощение ионов, пониженная проницаемость мембран, иммобилизация ионов в отдельных частях растений, удаление ионов из метаболических процессов с помощью образования запаса в нерастворимых формах в различных органах, адаптацию к замещению физиологического элемента токсичным в энзиме, удаление ионов из растений при вымывании через листья, соковыделении, сбрасывании листьев, выделении через корни. Толерантные растения могут стимулироваться при повышенных концентрациях металлов, что свидетельствует об их физиологической потребности в избытке. Отдельные виды растений способны-накапливать значительное количество тяжелых металлов без видимых признаков угнетения. Другие растения не имеют такой способности (см. табл.[ ...]
Давление является одним из основных факторов, определяющих производительность установок обратного осмоса. Производительность мембран увеличивается с повышением избыточного давления. Однако, начиная с некоторого давления, проницаемость мембран снижается вследствие уплотнения полимерного материала мембраны.[ ...]
Установлено также, что низкие ([ ...]
Поскольку полисахариды гемицеллюлоз имеют среднечисловой молекулярный вес не выше 30 000, применение обычной осмометрии затруднено вследствие проницаемости мембран для низкомолекулярных фракций. Предложенный Хиллом метод осмометрии в паровой фазе имеет ряд преимуществ перед другими методами. Этот метод основан на измерении разности давления паров раствора и растворителя и заключается в следующем . Каплю раствора и каплю растворителя помещают на два спая термопары и выдерживают в атмосфере, насыщенной парами чистого растворителя. Вследствие пониженного давления пара раствора часть пара сконденсируется на капле раствора, повышая температуру капли и термопары. Возникающая электродвижущая сила измеряется гальванометром. Верхний предел измеряемой величины молекулярного веса около 20 000, точность измерения 1 %.[ ...]
Наконец, мембраны эндоплазматического ретикулума - это те поверхности, по которым распространяются биотоки, являющиеся сигналами, меняющими избирательную проницаемость мембран и тем самым активность ферментов. Благодаря этому одни химические реакции пускаются в ход, другие тормозятся - обмен веществ подчиняется регуляции и протекает координированно.[ ...]
Нлазмалемма регулирует вход веществ в клетку и выход их из нее, обеспечивает избирательное проникновение веществ в клетку и из клетки. Скорость проннкновепия сквозь мембрану разных веществ различна. Хорошо проникают через нее вода и газообразные вещества. Легко проникают также жирорастворимые вещества,- вероятно, благодаря тому, что она имеет липидный слой. Предполагается, что липидный слой мембраны пронизан порами. Это позволяет проникать сквозь мембрану веществам, нерастворимым в жирах. Поры несут электрический заряд, поэтому проникновение через них ионов не вполне свободно. При некоторых условиях заряд пор меняется, и этим регулируется проницаемость мембран для ионов. Однако мембрана неодинаково проницаема и для разных ионов с одинаковым зарядом, и для разпых незаряжепных молекул близких размеров. В этом проявляется важнейшее свойство мембраны - избирательность ее проницаемости: для одних молекул и ионов она про-пицаема лучше, для других хуже.[ ...]
В настоящее время общепризнанным является механизм действия медиаторов в животных и растительных клетках, который основывается на регуляции ионных потоков. Изменения мембранных потенциалов обусловлены сдвигами ионной проницаемости мембран путем открытия или закрытия ионных каналов. С этим явлением и связаны механизмы возникновения и распространения ПД в животных и растительных клетках. В животных клетках - это №7К+-каналы, контролируемые ацетил-холином, и Са2+-каналы, чаще зависимые от биогенных аминов. В растительных клетках возникновение и распространение ПД связывается с кальциевыми, калиевыми и хлорными каналами.[ ...]
С большей воспроизводимостью и устойчивостью стабильный поток газов и паров может быть получен способами, основанными на диффузии газов или паров жидкости через капилляр (рис. 10) или проницаемую мембрану (рис. 11) в поток газа-разбавителя. В таких методах наблюдается равновесие между газовой фазой и адсорбирующими поверхностями аппаратуры, что обеспечивает стабильность микропотока.[ ...]
Увеличение температуры приводит к уменьшению вязкости и плотности раствора и одновременно к возрастанию его осмотического давления. Уменьшение вязкости и плотности раствора усиливает проницаемость мембран, а увеличение осмотического давления снижает движущую силу процесса и уменьшает проницаемость.[ ...]
В любой живой системе существует РЭП, и было бы удивительно, если бы не было. Это означало бы абсолютное равенство концентраций электролита во всех клетках, органах, наружных растворах либо полное совпадение величин проницаемости мембран ко всем катионам и анионам.[ ...]
В опыте 6, аналогичном опыту 1, определяли количество выделившегося калия и воднорастворимого органического вещества при разных концентрациях атразина. Судя по полученным результатам, можно сказать, что атразин не увеличивает проницаемость мембран для низкомолекулярных органических веществ и увеличивает для калия. Этот эффект был пропорционален концентрации атразина.[ ...]
При обследовании лиц, подвергавшихся во время работы действию радиации малого уровня (например, радиологи и техники, работающие с рентгеновским излучением, дозы которого измерялись индивидуальными дозиметрами) с помощью метода меченых атомов , проводились анализы крови на проницаемость мембран эритроцитов при прохождении одновалентных катионов. Было обнаружено, что проницаемость мембран эритроцитов у лиц, подвергавшихся облучению, значительно выше, чем у тех, кто не облучался. Кроме того, график зависимости позволил установить быстрое возрастание проницаемости при малом облучении; при больших дозах кривая становится пологой, аналогично наблюдению Стокке при изучении животных (см. рис. Х1У-3). Эти данные согласуются с результатами, полученными Петкау .[ ...]
При обессоливании минерализованных сточных вод гиперфильтрацией через полупроницаемые мембраны основные параметры - концентрацию растворенных веществ в концентрате и фильтрате необходимо определять на единицу ширины мембраны при заданной ее длине, разделяющей способности, коэффициенте проницаемости мембран, давлении, расходах исходной воды, фильтрата и концентрата.[ ...]
Возможность подобной адаптации обусловлена зависимостью термодинамических, .химических, кинетических констант от температуры. Эта зависимость, в общем, определяет направление и скорость химических реакций, конформационных переходов биологических маодомолекул,фазовых переходов липидов, изменение проницаемости мембран и других процессов, функционирование которых обеспечивает жизнедеятельность организмов при повышенной температуре.[ ...]
Все это пока лишь первые шаги в области применения омагниченной воды в медицине. Однако уже имеющиеся сведения свидетельствуют о перспективности применения омагничивания водных систем в этой области. Ряд медицинских проявлений возможно (гипотетически) связан с тем, что омагничивание водных систем повышает проницаемость мембран.[ ...]
Установлено, что полимерные пленки, выпускаемые промышленностью для ультрафильтрации, ионного обмена , а также мембраны из коллодия, желатины, целлюлозы и других материалов , имеют хорошую селективность, но малую проницаемость (0,4 л/м ч при давлении 40 am). Мембраны, приготовляемые по специальной прописи из смеси ацетатцеллюлозы, ацетона, воды, перхлората магния и соляной кислоты (соответственно 22,2; 66,7; 10,0; 1,1 и 0,1 весовых процента), позволяют опреснять воду с 5,25 до 0,05% NaCl и имеют проницаемость 8,5-18,7 л!м2 ■ ч при рабочем давлении 100-140 am , срок их службы не менее 6 месяцев . Электронно-микроскопические исследования этих мембран , так как, по предварительным расчетам 1192], обратный осмос может стать конкурентноспособным с другими способами опреснения воды при повышении проницаемости мембран до 5 м31мг в сутки.[ ...]
Потенциал покоя клеточной стенки. Клеточная стенка (оболочка) имеет отрицательный поверхностный заряд. Наличие этого заряда придает клеточной стенке отчетливо выраженные катионообменные свойства. Клеточная стенка характеризуется преимущественной избирательностью к ионам Са2+, который играет важную роль в регуляции проницаемости мембран по отношению к ионам К и №+.[ ...]
Таким образом, отмеченные эффекты указывают на то, что в культуральной жидкости микромицета Fusarium oxysporum помимо фузариевой кислоты содержатся и иные компоненты, обладающие высокой биологической активностью. Оценку степени патогенности различных изолятов фитопатогенных грибов можно производить на основе определения изменения проницаемости мембран растительных клеток к аммиаку.[ ...]
В результате снижается или прекращается новообразование АТФ, что ведет к подавлению процессов, зависящих от энергии дыхания. Нарушается также структура и избирательная проницаемость мембран, для поддержания которой необходима затрата энергии дыхания. Эти изменения приводят к снижению способности клеток поглощать и удерживать воду.[ ...]
С другой стороны, стабилизация пространственной структуры белка и других биополимеров осуществляется в значительной мере за счет взаимодействия: биополимер - вода. Основой функционирования живых систем считается водно-белково-нуклеиновый комплекс, поскольку только при наличии этих трех составляющих возможна нормальная жизнедеятельность мембран. Избирательная проницаемость мембран зависит от состояния воды. Экстраполируя кластерную модель воды на биологические системы, можно показать, что при разрушении кластера на определенны участках мембраны открывается путь для предпочтительного транспорта. Бесструктурная вода, например, препятствует повеДе нию протонов вблизи мембраны, тогда как по структурированно му каркасу протоны распространяются быстро.[ ...]
Описана схема непрерывного анализа газа с использованием ионоселективного электрода, которая может быть применена для определения содержания в газах НгЗ, НСЫ и НР. В обзоре работ НБС США среди других методов аттестации эталонных газов (смесей) указан также метод аттестации с помощью ионоселективных электродов для газов НСИ и НР. Из всех конструкций ионоселективных электродов обычно используют следующую: ионоселективная мембрана разделяет два раствора - внутренний и внешний (исследуемый). Для электрического контакта во внутренний раствор помещен вспомогательный электрод, обратимый к ионам внутреннего раствора, активность которых постоянна, вследствие чего постоянен и потенциал. На внутренней и внешней поверхностях мембраны возникает разность потенциалов, зависящая от разности активности ионов во внешнем и внутреннем растворах. Теория возникновения мембранного потенциала изложена в работе . В основном возникновение потенциала объясняется проницаемостью мембран либо только для катионов (катионоселективные), либо только для анионов (анионоселективные).
ПРОНИЦАЕМОСТЬ И ТРАНСПОРТ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ МЕМБРАНАХ
Проницаемость биологических мембран
Одна из важнейших функций биологической мембраны заключается в обеспечении обмена ионов и молекул между клеткой и окружающей средой. Способность биологических мембран пропускать через себя различные вещества называется проницаемостью . Изучение проницаемости клеток имеет большое значение, поскольку с данной функцией связаны практически все процессы жизнедеятельности клетки: метаболизм, генерация и проведение биопотенциалов, секреция, рецепция и т. д.
Транспорт веществ
Любая клетка очень точно поддерживает свой химический, в том числе и ионный состав. Постоянство ионного состава называется ионным гомеостазом и поддерживается за счёт транспорта веществ.
Транспорт веществ в организме можно разделить на три категории:
Дальний транспорт – перенос веществ между органами, его протяжённость в растениях может достигать нескольких десятков метров;
Ближний транспорт – перенос между соседними клетками;
Мембранный транспорт – перенос веществ через мембрану.
По энергетическим затратам мембранный транспорт можно разделить на 2 важнейших класса: активный и пассивный.
Пассивный транспорт не связан прямо с затратой химической энергии; он осуществляется в результате диффузии веществ в сторону меньшего электрохимического потенциала (где концентрация веществ и заряд меньше). Активный транспорт происходит при затрате химической энергии АТФ или переносе электрона по дыхательной цепи.
Виды пассивного транспорта веществ в клетках и тканях: диффузия, осмос.
Диффузия - основной механизм пассивного транспорта веществ, обусловленный наличием концентрационного градиента. Различают несколько видов диффузии:
1) простая диффузия, диффундирующее вещество движется по градиенту через мембрану, не образуя комплекса или проникая через канал;
2) облегченная диффузия , осуществляемая с помощью переносчиков - белков или молекулярных комплексов.
Простая диффузия- это самопроизвольный физический процесс проникновения вещества из области высокой в область меньшей его концентрации в результате теплового хаотического (броуновского) движения молекул.
С помощью простой диффузии через мембрану переносятся растворимые в липидах вещества, в частности такие хорошо растворимые в липидах и важнейшие для метаболического обмена вещества как кислород и углекислый газ. Через липидную фазу мембран в клетку могут проникать также яды и лекарства.
Математическое обоснование процесса диффузии впервые дал А. Фик. Согласно первому закону Фика поток вещества (J) прямо пропорционален градиенту концентрации dC/dx:
https://pandia.ru/text/78/170/images/image002_95.gif" width="433" height="56">
Учитывая это, формулу для потока вещества через мембрану можно записать в следующем виде:
https://pandia.ru/text/78/170/images/image004_68.gif" width="128" height="56">
Коэффициент проницаемости Р имеет размерность см/с и является количественной характеристикой способности конкретного вещества проникать через мембрану. Он аналогичен
коэффициенту диффузии (D), но зависит не только от природы вещества и температуры, но и от свойств мембраны.
DIV_ADBLOCK54">
Проникновение в клетку глюкозы, глицерина, аминокислот и некоторых других веществ не имеет линейной зависимости от их концентрации. Причем при определенных концентрациях скорость их проникновения значительно выше, чем при простой диффузии. Эта особенность объясняется тем, что в данном случае наблюдается не простая, а облегченная диффузия. Вещество самостоятельно диффундирует через мембрану, но скорость диффузии намного возрастает, если молекулы этого вещества образуют комплекс с молекулами переносчика, который хорошо растворяется в липидах. Молекулы-переносчики могут быть как подвижными, так и фиксированными в мембране - каналы .
Диффузия с участием переносчика, как и простая, происходит до тех пор, пока концентрация по обе стороны мембраны не станет одинаковой.
Разновидностью облегченной диффузии является так называемая обменная диффузия , при которой переносчик образует соединении с диффундирующим веществом и перемещается с ним от одной поверхности мембраны к другой, где молекула переносчика освобождается, ее место занимает другая молекула того же вещества и комплекс переносится обратно. При работе переносчиков в случае обменной диффузии концентрация веществ по обе стороны мембраны не изменяется. Существование обменной диффузии было доказано методом меченых атомов на эритроцитах, митохондриях и др.
Проникновение растворенных частиц, обладающих электрическим зарядом, через клеточную мембрану осуществляется по электрохимическому градиенту , а не по концентрационному.
Электрохимический потенциал – энергия, которую надо затратить для перемещения одного моля вещества из бесконечно удалённой точки пространства в данную точку с конкретными условиями.
Величина электрохимического потенциала описывается формулой:
где: - стандартный член;
Активность j-го иона
Химическая работа;
Парциальный моляльный обьем;
Механическая работа (работа по расширению объёиа)
Заряд иона;
Электрический потенциал;
Число Фарадея;
Электрическая работа.
Молекулы вещества всегда двигаются в сторону своего более низкого электрохимического потенциала.
Потенциал Нернста
Рассмотрим простую систему, представляющую собой два отсека, содержащие раствор соли (например, KCl) и разделённые мембраной, которая пропускает только катион, в нашем случае К+.

Растворы находятся в равновесии, это означает, что электрохимические потенциалы ионов в обоих отсеках одинаковы. Математически это будет выражаться уравнением:
Это уравнение, учитывая, что давления и моляльные объёмы вещества в обоих отсеках одинаковы, позволяет нам рассчитать разность электрических потенциалов между отсеками:

Это уравнение называется уравнением Нернста. Если учесть значения констант перед знаком логарифма, и вместо натуральных логарифмов использовать десятичные, то эту формулу можно записать в виде:
https://pandia.ru/text/78/170/images/image020_2.jpg" width="459" height="268">
Осмотическое давление раствора зависит от количества растворенных ионов и температуры. В соответствии с уравнением Вант-Гоффа осмотическое давление (π) раствора прямо пропорционально концентрации (С) растворенного вещества и абсолютной температуре раствора (T):
π = iRTC,
где i - изотонический коэффициент, зависящий от степени диссоциации электролита и показывающий, во сколько раз увеличивается количество растворенных частиц при диссоциации молекул; для неэлектролитов i = l, для электролитов i > 1; R - газовая постоянная.
Активный транспорт - движение против градиента электрохимического потенциала, осуществляемое с затратой химической энергии за счёт гидролиза АТФ или переноса электрона по дыхательной цепи.
Выделяют первично-активный и вторично-активный транспорт.
Рис. - Активный перенос ионов при работе транспортных АТФ-аз.
Транспорт называется первично-активным , если он осуществляется белками-переносчиками (они ещё называются ионными насосами), источником энергии для которых служат АТР, пирофосфат или субстраты, окисляемые в электрон-транспортных цепях митохондрий, хлоропластов.
Типичный пример первично-активного транспорта - активный транспорт ионов с помощью АТФ-аз.
Вторично-активным (сопряженным) транспортом называют процесс переноса ионов через мембрану против градиента его концентрации за счет энергии электрохимического градиента других ионов. Сопряженный транспорт может осуществляться в режиме симпорта (оба иона переносятся через мембрану в одном направлении) или антипорта (ионы транспортируются в противоположных направлениях). Вторично-активный транспорт обеспечивает мембранный перенос моносахаридов, сахарозы, аминокислот, пептидов, анионов и ряда катионов. Для этой цели мембранные белки-переносчики чаще всего используют электрохимический градиент ионов водорода , создаваемый различными Н+-насосами.

Рис. - Сопряженный транспорт ионов и веществ через мембраны (Δφ - разность потенциалов, ΔрН - разность концентрации протонов)
Между пассивными и активными потоками в клетке существует взаимодействие, направленное на поддержание постоянства ионного состава клетки.
При блокировании энергетики клетки (пониженной температурой, ингибиторами, темнотой) интенсивность активного транспорта снижается, приток ионов из внешней среды уменьшается. Одновременно наблюдается возрастание электрического сопротивления мембраны в десятки раз. Это свидетельствует об уменьшении транспорта ионов по пассивным каналам, что предотвращает потерю ионов, находящихся в клетке.